

SWI/SNF复合物是一类重要的染色质重塑复合物,通过借助核心亚基BRG1水解ATP获取的能量动员核小体,实现染色质重塑,进而调控基因表达。SWI/SNF复合物多个成员在肿瘤中广泛存在高频突变,其中亚基ARID1A的编码基因突变频率最高,常表现为失活突变,作为抑癌基因参与肿瘤的发生和发展。以往研究已证实ARID1A缺陷会促使肝癌转移,但具体的作用机制仍不明晰。
2021年10月23日,Cell Death & Disease在线发表了上海交通大学系统生物医学研究院韩泽广团队题为“ARID1A deficiency weakens BRG1-RAD21 interaction that jeopardizes chromatin compactness and drives liver cancer cell metastasis”的最新研究成果。该研究揭示了ARID1A调控染色质构象的新机制,并从染色质三维结构改变层面探究了ARID1A缺陷驱动肝癌细胞转移的分子机理。

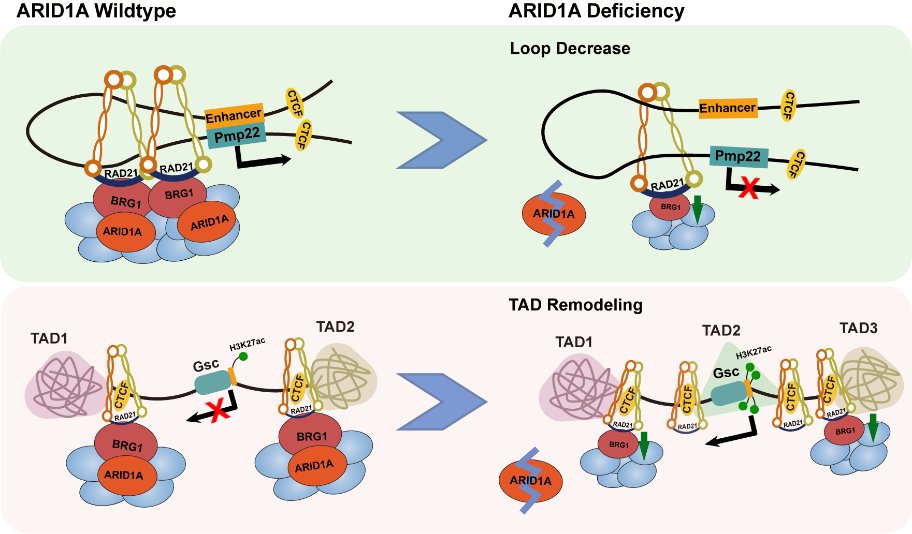
在真核生物中,DNA并不是以线性分子的形式存在,而是按照严格的层级结构包装成染色质,有序排布在细胞核内。DNA缠绕组蛋白八聚体形成核小体颗粒,核小体串联成直径约10nm的染色质纤维构成染色质初级结构,染色质纤维进一步卷曲折叠最终构成复杂的染色质三维结构。对全基因组表观遗传标记分析发现,常染色质和异染色质结构在染色体上呈交替出现,借助染色质构象捕获技术(Hi-C)绘制的空间互作矩阵呈现出“格子”或“棋盘”模式,为相互独立的染色质区室(chromatin compartment);在数十到数百kb碱基的尺度上,染色质折叠形成相较于邻近的染色质更为紧密的拓扑相关结构域(topologically associating domain, TAD),相邻的TAD边界由CTCF和cohesin复合物负责维护;空间邻近的接触互作对被称作染色质环(chromatin loop),是基因表达调控的结构和功能单元。该研究首先通过分析ARID1A野生型和缺失型小鼠肝脏细胞的染色质构象发现,ARID1A缺失会导致染色质不同层级结构均发生改变,表现为近12.1%的区室类型转变、TAD数量减少且平均长度显著增加、TAD间边界强度减弱以及染色质环数量减少。借助体内外免疫沉淀等方法进一步分析证实,SWI/SNF复合物核心元件BRG1与cohesin复合物亚基RAD21之间存在直接的相互作用,敲除ARID1A会导致BRG1蛋白表达以及与RAD21互作的BRG1显著减少,这也是ARID1A缺陷引起染色质构象改变的重要分子机制。此外,结合转录谱发现,区室转变基因与其转录水平改变呈显著相关性,且这类基因富集在细胞外基质、细胞迁移和黏附等信号通路。其构象调控方式可归纳为:染色质环减少或被阻断(A-B转变)以及TAD重塑(B-A转变)。功能试验发现,ARID1A缺陷通过介导空间构象改变,调控肿瘤相关基因转录(例如:PMP22, GSC),促进肝癌细胞的转移。本研究为首次探究SWI/SNF复合物重要组分ARID1A在肝脏细胞染色质构象调节中发挥的作用,并揭示其作用方式和分子基础;同时从染色质三维结构层面提出ARID1A缺陷驱动肝癌细胞转移的新机制。
上海交通大学系统生物医学研究院韩泽广教授、石毅副研究员为本研究的通讯作者,2016级博士研究生尚雪莹、石毅副研究员和2017级硕士研究生何丹丹为本项研究的共同第一作者。
原文链接:https://www.nature.com/articles/s41419-021-04291-6
稿件来源:韩泽广课题组
图文编辑:王华瑶