

近日,上海交大吴方课题组在线发表最新科研成果“A pharmacological probe identifies cystathionine β-synthase as a new negative regulator for ferroptosis”该论文发表在Nature集团《Cell Death and Disease》杂志Chemical Biology领域。
小分子化合物调控蛋白质大分子的功能是生命现象的本质之一。因此,发现具有生物活性的小分子调控物不仅能控制细胞内生命过程,也可发现蛋白质的新功能。天然免疫抑制药物雷帕霉素(Rapamycin)在细胞内的靶点蛋白mTOR(Mammalian Target of Rapamycin), 在免疫抑制和肿瘤治疗中具有重要作用,是生命过程的核心分子,也是生命医学研究的热点。
吴方课题组,前期建立了硫化氢气体产生酶的新型高通量筛选方法(Zhou Y. et al., Chemical Communications 2013),从近3万多个小分子化合物中筛选发现了9个合成小分子和2个天然产物是硫化氢产生酶CBS的抑制剂(Zhou Y. et al., Chemical Communications 2013;王莉等 生物技术 2017)。近期,通过与中国药科大学徐进宜教授合作,使用药物设计和药物化学方法,成功获得高效CBS抑制剂CH004(IC50约为1 micromolar),该抑制剂比已知CBS抑制剂AOAA的细胞有效性提高近1000倍。
进一步研究发现,该抑制剂可以高效抑制多种肿瘤细胞的增殖,在小鼠肝癌异种移植模型上也展现了良好的体内抗肿瘤增殖活性。有趣的是,该抑制剂可以诱导HepG2细胞和MEF细胞铁死亡,且这种诱导机制不同于已知铁死亡诱导物Erastin。这一发现,揭示CH004的靶点CBS是铁死亡的新型负调蛋白。
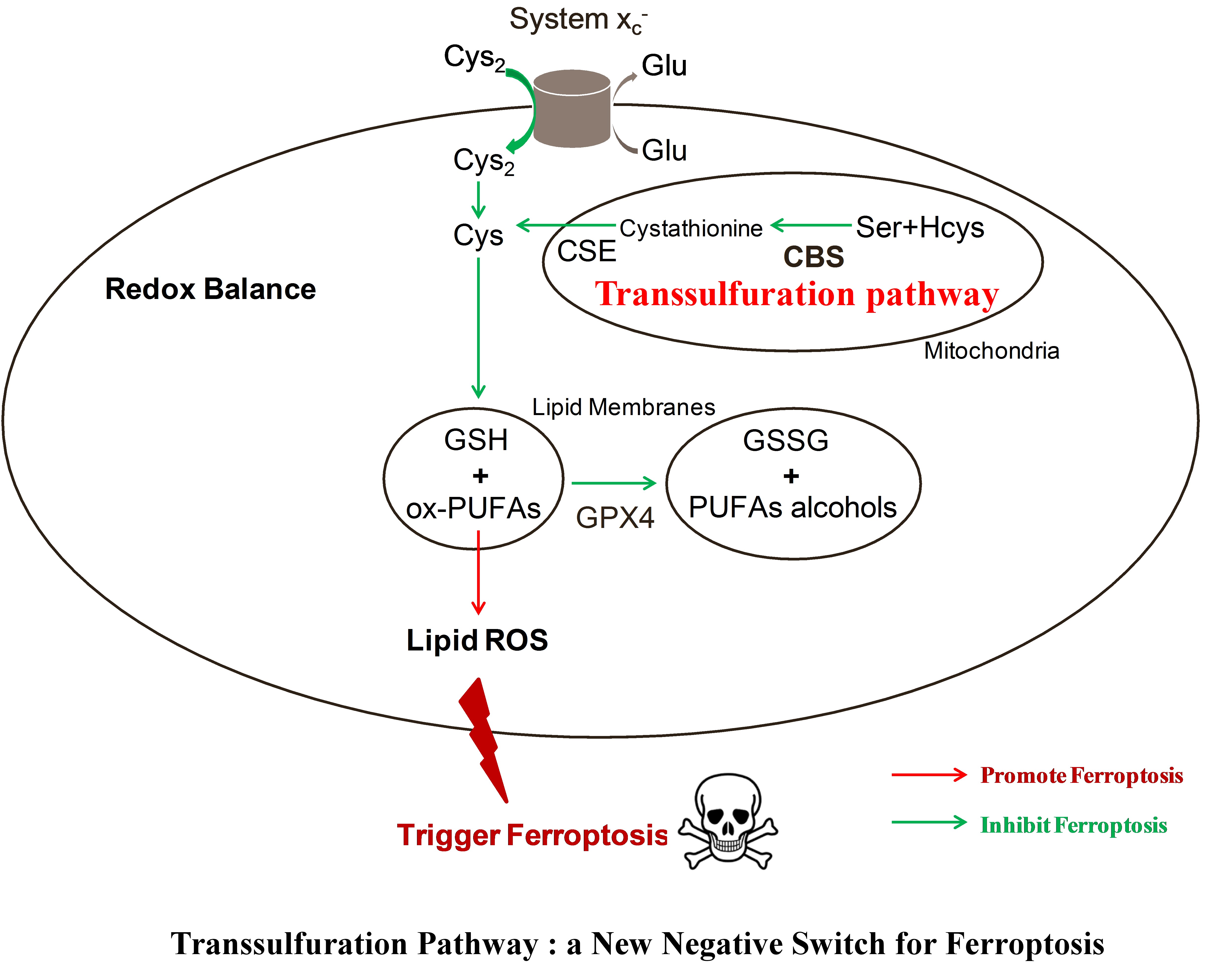
铁死亡是新近发现的一种不同于凋亡的细胞死亡方式,前人研究发现胱氨酸/谷氨酸转运蛋白System Xc-通过摄取细胞外胱氨酸来抑制细胞铁死亡的发生。本研究中,我们利用药理性探针工具,率先揭示调控细胞内的半胱氨酸途径也可以调控细胞铁死亡的进程,硫化氢产生酶CBS具有负调铁死亡进程的新功能。这一研究,不仅为研究硫化氢气体信号通路提供药理性探针工具,也为肿瘤等疾病的治疗提供了新机制和药物靶点。
吴方课题组2017届硕士毕业生王莉为主要完成人(第一作者),中国药科大学博士毕业生蔡浩为本文共同第一作者。
原文链接:https://www.nature.com/articles/s41419-018-1063-2
编辑:王华瑶